Chemische Untersuchungen im Kontext von Feuchteschäden und Schimmelpilzbefall umfassen neben der Bestimmung des pH-Wertes vor allem qualitative und quantitative Salzanalysen. Hierbei geht es um die Bestimmung der Art und Konzentration bauschädigender Salze Salze bestehen aus positiv geladenen und negativ geladenen Ionen. Zwischen diesen Ionen liegen ionische Verbindungen vor. Salz hat eine kubische wie z. B. Carbonate, Sulfate, Chloride Chloride sind Salze der Salzsäure. Sie zählen zur Gruppe der bauschädigenden Salze und treten in Gebäuden oft im Sockel- bzw. und Nitrate. Diese Salze verursachen u. a. die Hygroskopizität von Baustoffen – also die Fähigkeit, Feuchtigkeit aus der Umgebungsluft aufzunehmen und zu speichern. Zudem verhindern die Hygroskopizität die Austrocknung von Baustoffen, so dass eine höhere Feuchtigkeit im Untergrund vorliegt. Dies wiederum kann das Wachstum von Schimmelpilzen fördern, da einige Arten auch auf salzbelasteten Untergründen ansiedeln können. Diese Schimmelpilzarten werden als alkalophil bezeichnet.
Vor Ort können einfache, so genannte halbqualitative, Salzanalysen ( pH-Wert Mit dieser Maßzahl wird die Stärke einer Säure oder Lauge bezeichnet, d. h. der pH-Wert sagt aus, wie sauer bzw. -Bestimmung) mittels Teststreifen durchgeführt werden. Hierbei wird die zu prüfende wässrige Lösung in einem Messgefäß mit drei Tropfen einer pH-Indikatorlösung versetzt. Durch Farbreagenzien kann nachgewiesen werden, welche Anionen oder Kationen sich in der Lösung befinden. Der dabei auftretende typische Farbwert wird mit einer beigefügten Farbskala verglichen und kann nach einer einfachen Methode bewertet werden (z. B. Null für nicht vorhanden, 1 = geringe Konzentration, 2 = mittlere oder durchschnittliche Konzentration, 3 = hohe bis starke Konzentration und 4 = sehr starke bis überdurchschnittliche Konzentration).
Wenn der Salzgehalt quantitativ nachgewiesen werden soll (Bestimmung eines Salzmoleküls oder einer Salzmischung mit den zugehörigen Kationen), sind diese Teststreifen ungeeignet. Dann müssen Materialproben (z. B. Bohrmehl oder Steinproben) labortechnisch untersucht werden z. B. über nass-chemische Verfahren, die heute immer weniger eingesetzt werden sowie aufwändige Methoden wie z. B. Ionenchromatographie Die Ionenchromatographie ist eine vielseitige Analysemethode zur qualitativen und quantitativen Erfassung von anionischen Spezies mit Hilfe von Trennsäulen und Detektoren. , Röntgendiffraktometrie oder Infrarotspektroskopie Jede Verbindung und insbesondere jede organische Verbindung zeigt bei Anregung mit Infrarotlicht ein spezifisches Molekülschwingungsverhalten. Dieses Verhalten erzeugt materialcharakteristisch typische , die für die alltägliche Bauwerks- und Innenraumdiagnostik nicht praktikabel und zu teuer sind.
Für die Salzanalysen werden Proben von Bohrkernen oder -mehl, Putz- oder Steinproben entnommen. Wichtig ist, dass nicht nur Salzanalysen in dem Bauteilbereich durchgeführt werden, in denen eine starke Salzbelastung sichtbar ist. Besonders leicht lösliche Salze wandern über die Kapillarität Die Saugfähigkeit eines (Bau)Stoffes gegenüber Wasser und anderen Flüssigkeiten wird als Kapillarität bezeichnet. Die kapillare Leitfähigkeit hängt im Wesentlichen von in die oberen Bauteilbereiche, so dass auch in 1 bis 2 Meter Höhe Salze im Wandquerschnitt nachgewiesen werden. Schwer lösliche Salzverbindungen werden sich dagegen im unteren Bauteilbereich nachweisen lassen. Sollen nur die in Wasser löslichen Salze analysiert werden, muss die Baustoffprobe nach dem Zerkleinern nur mit Wasser extrahiert werden. Muss allerdings die Gesamtmenge der Salzbelastung bestimmt werden, ist es notwendig, einen Sodaauszug zu nehmen. Das entsprechende Filtrat der Extraktion oder des Sodaauszugs wird dann weiter analysiert.
Carbonate werden durch die Reaktion mit verdünnter Salzsäure nachgewiesen. Fügt man einem Teil der wässrigen Lösung vorsichtig verdünnte Salzsäure hinzu, schäumt dies bei Anwesenheit von löslichem Carbonat auf. Dieses Aufschäumen wird durch die frei werdende Kohlensäure verursacht und ist ein Hinweis auf die Anwesenheit von Soda oder Pottasche. Liegen Carbonate wie z. B. bei Kalk- oder Kalkzementputzen als natürlich vorkommendes Bindemittel vor, kann diese Salzanalyse nicht durchgeführt werden.
Sulfate können als Natrium-, Kalium- oder auch als Magnesiumsulfat vorliegen. Für diesen Test wird im Reagenzglas eine Baustoffprobe mit verdünnter Salzsäure aufgelöst. Anschließend wird diese filtriert. Um die Löslichkeit zu erhöhen, kann die Probe auch mit dem Brenner erhitzt werden. In einem zweiten Reagenzglas wird eine Messerspitze Bariumchlorid in destilliertem Wasser gelöst. Die beiden Flüssigkeiten werden vorsichtig zusammengeschüttet. Der Sulfatgehalt wird durch einen sehr feinkristallinen weißen Niederschlag (Bariumsulfat) angezeigt. Die früher sehr aufwendige Bestimmungsmethode, durch geeignete Fällungsreaktionen Sulfat nachzuweisen, kann mittlerweile durch einfache Bestimmungsmethoden mittels Teststäbchen ersetzt werden. Die Teststäbchen sind in vier Zonen eingeteilt und enthalten unterschiedliche Mengen des rot gefärbten Thorium-Barium-Komplexes, der bei Anwesenheit der entsprechenden Mengen Sulfationen in das gelb gefärbte Thorium umschlägt. Der pH-Wert der zu prüfenden Lösung soll bei 4 bis 8 liegen. Alkalische Lösungen (pH-Wert > 8) müssen durch Zugabe von organischen Säuren eingestellt werden.
Chloride können als Natrium-, Kalium- oder als Calciumchlorid vorliegen. Der Nachweis erfolgt in einem Reagenzglas mit verdünnter Schwefelsäure unter Verwendung eines Brenners, mit dem die Baustoffprobe erhitzt wird. Salzsäure darf zum Lösen nicht verwendet werden, da diese sonst mit ihren Chlorid-Anionen das Ergebnis beeinflussen würde. Nach dem Filtrieren wird langsam Silbernitrat hinein getröpfelt, um die gewünschte Reaktion in Gang zu setzen. Das Chlorid zeigt sich durch einen voluminösen weißen, flockigen Niederschlag (Silberchlorid).
Die Salze der Salpetersäure liegen meist als Natrium-, Kalium- oder Calciumnitrat vor. Die Baustoffprobe wird im Reagenzglas mit verdünnter Salzsäure gelöst und filtriert. Dieser Vorgang kann ebenfalls durch Erhitzen beschleunigt werden. Anschließend werden einige Kristalle Eisen(II)-sulfat sowie einige Tropfen verdünnter Schwefelsäure zugegeben. Nach dem Abkühlen wird das Reagenzglas leicht geneigt, um sehr vorsichtig mit der Pipette konzentrierte Schwefelsäure unter zu mischen. Nitrat zeigt sich durch einen an der Grenzschicht zwischen konzentrierter Schwefelsäure und Baustofflösung entstehenden braunen bis violett braunen Ring. Hierfür steht ein Nitrat-Teststäbchen zur Verfügung.
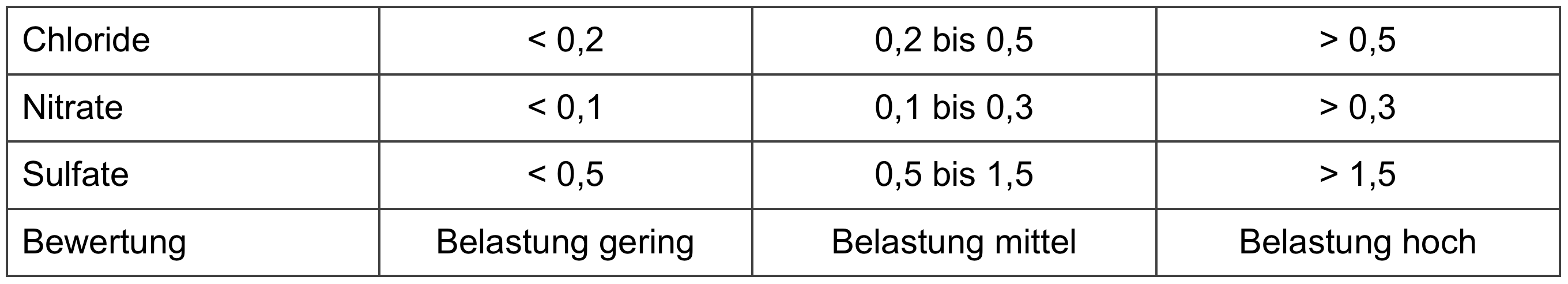
Aufgrund der ermittelten Werte wird der Versalzungsgrad als „gering“, „mittel“ oder „hoch“ eingestuft. Dabei ist der ermittelte höchste Gehalt an Salz-Ionen (unabhängig ob Chlorid, Nitrat oder Sulfat) maßgebend.
In einigen Fällen kann es notwendig sein, die Versalzung in Baukonstruktionen nach ihrer räumlichen Verteilung zu bestimmen (z. B. die Salzverteilung im Mauerwerksquerschnitt). Hierfür stehen sehr aufwändige Verfahren zur Verfügung, die im Rahmen der alltäglichen Bauwerks- und Innenraumdiagnostik allerdings nicht praktikabel und zu teuer sind wie z. B. die Ionenchromatographie und die Röntgendiffraktometrie.
Die Ionenchromatographie ist eine analytische Methode zur Trennung von Stoffen. Bei dieser Methode wird eine Messung mit einer Standardlösung durchgeführt (= Nullprobe). In dieser Lösung befindet sich eine bekannte Menge an nachzuweisenden Ionen. Im Verlauf der Analyse Unter Analyse werden allgemein Untersuchungen verstanden, die das Zusammenspiel und die Abhängigkeit (Ursache-Wirkung) zwischen der Art, dem Ort und dem werden kontinuierlich Leitfähigkeitsmesswerte der Probe in regelmäßigen kleinen Zeitabschnitten auf einen Computer übertragen. Die Leitfähigkeit wird in einem Diagramm gegen die Zeit aufgetragen, so dass sich so genannte „Peaks“ in Form einer Kurve ergeben. Danach werden die Flächen dieser Peaks, die durch das Verlängern der Grundleitfähigkeitslinie entstehen, ins Verhältnis zu der Konzentration, die aus der Nullprobe bekannt ist, gesetzt. Bei Analyse einer unbekannten Probe kann aus der Fläche der Peaks die Konzentration des nachzuweisenden Ions ermittelt werden.
Mit der Röntgendiffraktometrie können Beugungsphänomene von Röntgenstrahlungen gemessen werden. Diese werden in der Kristallographie (= Wissenschaft über die Struktur, Entstehung oder Herstellung sowie Eigenschaften und Anwendungen von Kristallen) zur Strukturanalyse eingesetzt. Das Messprinzip basiert darauf, dass die Wellenlänge der Röntgenstrahlung im Bereich eines Atomabstandes (0,1 bis 0,3 nm) liegt. Da Salze sehr viele Reflexlinien aufweisen können, sind der Interpretation von Röntgendiagrammen insbesondere bei Salzgemischen Grenzen gesetzt. Darüber hinaus sind Salze bekannt, die kryptokristallin (= unter dem Mikroskop nicht mehr aufzulösen) sind und infolgedessen röntgenamorph (= nicht mehr ermittelt werden können) auftreten.
Einige Salze können auch mithilfe der Infrarotspektroskopie analysiert werden, allerdings sind dem Verfahren vor allem bei Mischsalzen Grenzen gesetzt. Das Rasterelektronenmikroskop Die Rasterelektronenmikroskopie (REM) ist die vielseitigste unter den mikroskopischen Untersuchungsmethoden. Das Rasterelektronenmikroskop ist ein Verfahren zur Abbildung von Oberflächen und kann ebenfalls für Salzanalysen eingesetzt werden. Allerdings bringen REM Siehe Rasterelektronenmikroskop. -Aufnahmen keinen Mehrwert bei der qualitativen oder quantitativen Salzbestimmung. Sie können allerdings verwendet werden, um z. B. Salzkristalle in Poren- oder Hohlräumen wie z. B. in Putzgefügen, Betonen oder Natursteinen zu dokumentieren.
Der Vollständigkeit halber soll noch die Photometrie erwähnt werden. Hierbei handelt es sich um ein Messverfahren, mit dem der Wellenlängenbereich des ultravioletten und des sichtbaren Lichts ermittelt werden kann. Das nach der Extraktion oder nach dem Sodaauszug erhaltene Filtrat wird mit Reagenzien versetzt, die spezifisch auf die einzelnen Anionen farbig reagieren. Um die Konzentration dieser Lösung zu messen, wird ein Wellenlängenbereich gewählt, der von den zu bestimmenden Molekülen oder Ionen absorbiert wird, allerdings nicht von anderen Bestandteilen. Mit dieser Messmethode können Reihenuntersuchungen z. B. über die Konzentration an Chlorid-, Sulfat- und Nitrationen sowie in einzelnen Fällen auch der Nitrit-, Carbonat- oder Phosphatgehalt kostengünstig durchgeführt werden.